ثابت معدل التفاعل
ثابت معدل التفاعل في الكيمياء (بالإنجليزية: reaction rate constant ) هو ثابت يحدد سرعة جريان تفاعل كيميائي ويرمز له بالرمز k أو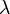 .[1]
.[1]
ففي تفاعل كيميائي حيث تتفاعل مادتين A و B وتنتجان مركبا C , يكون معدل التفاعل :
التفاعل: A + B → C
حيث (k(T ثابت معدل التفاعل وهو يعتمد على درجة الحرارة.
في المعادلة أعلاه تعني [C] تركيز المادة C بوحدة مول لحجم معين من المحول باعتبار أن التفاعل يسير في محلول (بالنسبة لتفاعل يجري على سطح فتعبر C عن عدد المولات على السطح) .
وتعبر قوتي الأس m و n في المادلة عن درجة التفاعل وطريقة سيره . ويمكن تعيين كل منهما عمليا .
بالنسبة إلى تفاعل يجري في خطوة واحدة يمكننا كتابته في الصيغة:

حيث:
Ea طاقة تنشيط ، R ثابت الغازات العام.
ونظرا لان درجة الحرارة تعطي طاقة للجزيئات طبقا توزيع بولتزمان ، فينتج عن ذلك تغير في معدل الاصتدامات التي تجري عند طاقة أعلى من Ea طبقا للدالة الأسية e-Ea/RT. ويسمى A معامل التردد.
وتعطينا معادلة أرينيوس مقادير العلاقة بين طاقة التنشيط و معدل التفاعل الذي يسير عليهما التفاعل .
تعتمد وحدات معدل التفاعل على درجة التفاعل: [2]
(أي مول1-n·لترn-1·ثانية-1)
ثابت معدل التفاعل في الكيمياء (بالإنجليزية: reaction rate constant ) هو ثابت يحدد سرعة جريان تفاعل كيميائي ويرمز له بالرمز k أو
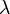 .[1]
.[1]ففي تفاعل كيميائي حيث تتفاعل مادتين A و B وتنتجان مركبا C , يكون معدل التفاعل :
التفاعل: A + B → C

حيث (k(T ثابت معدل التفاعل وهو يعتمد على درجة الحرارة.
في المعادلة أعلاه تعني [C] تركيز المادة C بوحدة مول لحجم معين من المحول باعتبار أن التفاعل يسير في محلول (بالنسبة لتفاعل يجري على سطح فتعبر C عن عدد المولات على السطح) .
وتعبر قوتي الأس m و n في المادلة عن درجة التفاعل وطريقة سيره . ويمكن تعيين كل منهما عمليا .
بالنسبة إلى تفاعل يجري في خطوة واحدة يمكننا كتابته في الصيغة:

حيث:
Ea طاقة تنشيط ، R ثابت الغازات العام.
ونظرا لان درجة الحرارة تعطي طاقة للجزيئات طبقا توزيع بولتزمان ، فينتج عن ذلك تغير في معدل الاصتدامات التي تجري عند طاقة أعلى من Ea طبقا للدالة الأسية e-Ea/RT. ويسمى A معامل التردد.
وتعطينا معادلة أرينيوس مقادير العلاقة بين طاقة التنشيط و معدل التفاعل الذي يسير عليهما التفاعل .
محتويات
- 1 وحدات
- 2 البلازما و الغازات
- 3 اقرأ أيضا
- 4 المراجع
وحدات
{مقالة : درجة التفاعل}تعتمد وحدات معدل التفاعل على درجة التفاعل: [2]
- بالنسبة إلى تفاعل من الدرجة صفر ، يتخذ المعدل وحدات mol·L-1·s-1
- وبالنسبة إلى الدرجة 1 ، يتخذ المعامل الوحدة: s-1
- وبالنسبة إلى تفاعل من الدرجة الثانية , يتخذ المعامل الوحدات : L·mol-1·s-1
- بالنسبة إلى الدرجة n للتفاعل يتخذ المعدل وحدات mol1-n·Ln-1·s-1
(أي مول1-n·لترn-1·ثانية-1)

