تقدم تفاعل
تقدم تفاعل (بالإنجليزية: Extent of reaction) يعطي كمية التغير الكيميائي من الحالة البدئية إلى حالة التوازن. ويعطي التقدم نحو التوازن وفق ثابت التوازن والشروط البدئية للتفاعل.[1]
التقدم هو حاصل قسمة الفرق بين كمية مادة في حالة تقدم معينة لتفاعل كيميائي وكميتها في الحالة البدئية مقسومة على معامل قياس اتحادية العناصر لها الذي يكون ذا إشارة سالبة إذا كانت المادة من المتفاعلات ، وذا إشارة موجبة إذا كانت من النواتج.
ξ = (ni - ni,0) / vi
 A يتفاعل فيصبح B
A يتفاعل فيصبح B
فيكون
ξ == 0 للمادة الداخلة في التفاعل A (الحالة الأولية), بينما تكون ξ == 1 مول للحالة النهائية B ، ومعناها أن 1 مول A اختفى ونتج 1 مول B (الحالة النهائية).
عندما يسير التفاعل بالكامل وخصوصا إذا كان التفاعل سريعا فلا يهم تقدم التفاعل ، ولكنه يهمنا في التفاعلات التي تتم ببطء والتفاعلات التي لا تكتمل وحالات الاتزان.
 C يوجد في حالة توازن مع D
C يوجد في حالة توازن مع D
هنا يصف تقدم التفاعل كميات المواد عند نهاية التفاعل والوصول إلى حالة التوازن وتغير كميات المواد خلال التفاعل مع الزمن.

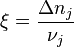
ويتضح من تلك المعادلة ان معاملات حساب العناصر المتفاعلة تكون شبه لا بعدية حيث تنتج وحدة في شكل . وكما نرى يتخذ تقدم التفاعل قيما موجبة ، ذلك مع استخدام النظام المتبع في حساب العناصر المتفاعلة (معاملات سلبية للعناصر الداخلة في التفاعل ومعاملات موجبة للمركبات الناتجة).
. وكما نرى يتخذ تقدم التفاعل قيما موجبة ، ذلك مع استخدام النظام المتبع في حساب العناصر المتفاعلة (معاملات سلبية للعناصر الداخلة في التفاعل ومعاملات موجبة للمركبات الناتجة).

ونحصل لهذا التفاعل على "التقدم" الآتي:

حيث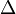 تعني التغير.
تعني التغير.
ويمكن تعيين سرعة تفاعل كيميائي بواسطة تقدم التفاعل كالآتي:
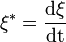
[*]^ (إنجليزية) The Advancement of a Reaction; Advancement, Stress, and Chemical Equilibrium. Lecture - University of Florida
[/list]
تقدم تفاعل (بالإنجليزية: Extent of reaction) يعطي كمية التغير الكيميائي من الحالة البدئية إلى حالة التوازن. ويعطي التقدم نحو التوازن وفق ثابت التوازن والشروط البدئية للتفاعل.[1]
التقدم هو حاصل قسمة الفرق بين كمية مادة في حالة تقدم معينة لتفاعل كيميائي وكميتها في الحالة البدئية مقسومة على معامل قياس اتحادية العناصر لها الذي يكون ذا إشارة سالبة إذا كانت المادة من المتفاعلات ، وذا إشارة موجبة إذا كانت من النواتج.
ξ = (ni - ni,0) / vi
محتويات
- 1 التفاعلات البسيطة
- 2 تفاعلات في حالة اتزان
- 3 تعريف بالرياضيات
- 4 مثـــال
- 5 المصادر
- 6 اقرأ أيضا
- 7 مراجع
التفاعلات البسيطة
نفترض التفاعل : A يتفاعل فيصبح B
A يتفاعل فيصبح Bفيكون
ξ == 0 للمادة الداخلة في التفاعل A (الحالة الأولية), بينما تكون ξ == 1 مول للحالة النهائية B ، ومعناها أن 1 مول A اختفى ونتج 1 مول B (الحالة النهائية).
عندما يسير التفاعل بالكامل وخصوصا إذا كان التفاعل سريعا فلا يهم تقدم التفاعل ، ولكنه يهمنا في التفاعلات التي تتم ببطء والتفاعلات التي لا تكتمل وحالات الاتزان.
تفاعلات في حالة اتزان
نفترض التفاعل التالي من حالة اتزان C يوجد في حالة توازن مع D
C يوجد في حالة توازن مع Dهنا يصف تقدم التفاعل كميات المواد عند نهاية التفاعل والوصول إلى حالة التوازن وتغير كميات المواد خلال التفاعل مع الزمن.

- dnj: التغير التفاضلي لكمية المادة j
- νj: معاملات العناصر المتفاعلة للمادة j
(للتفاعل A + 3 B → 2 C + 4 D ; تكون νA == -1 وνB = -3 وνC = 2 وνD == 4) - dξ: التغير التفاضلي لتقدم التفاعل ξ
تعريف بالرياضيات
إذا تغير تقدم التفاعل بالمقدار dξ (تعني d تغير طفيف جدا ، أي تغير تفاضلي) فتتغير بذلك أيضا كمية المادة n بالمقدار dn. وبتعديل المعادلة نحصل على تعريف تقدم التفاعل: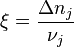
- ξ: تقدم التفاعل
- Δnj: التغير في اكمية المادة j
- νj: معامل المادة j
ويتضح من تلك المعادلة ان معاملات حساب العناصر المتفاعلة تكون شبه لا بعدية حيث تنتج وحدة في شكل
 . وكما نرى يتخذ تقدم التفاعل قيما موجبة ، ذلك مع استخدام النظام المتبع في حساب العناصر المتفاعلة (معاملات سلبية للعناصر الداخلة في التفاعل ومعاملات موجبة للمركبات الناتجة).
. وكما نرى يتخذ تقدم التفاعل قيما موجبة ، ذلك مع استخدام النظام المتبع في حساب العناصر المتفاعلة (معاملات سلبية للعناصر الداخلة في التفاعل ومعاملات موجبة للمركبات الناتجة).مثـــال
يختص كل تفاعل بتقدم للتفاعل ، ويتبين ذلك من المثال الآتي:
ونحصل لهذا التفاعل على "التقدم" الآتي:

حيث
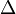 تعني التغير.
تعني التغير.ويمكن تعيين سرعة تفاعل كيميائي بواسطة تقدم التفاعل كالآتي:
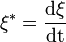
- ξ*: معدل التفاعل
- dξ: التغير التفاضلي لتقدم التفاعل
- dt: التغير التفاضلي للزمن
المصادر
[list=references][*]^ (إنجليزية) The Advancement of a Reaction; Advancement, Stress, and Chemical Equilibrium. Lecture - University of Florida
[/list]

